中大新聞中心
中大学者研植物细胞自噬机制取得重大突破成果登《美国科学院院报》
由香港中文大学(中大)生命科学学院卓敏生命科学教授姜里文教授带领的科研团队,最近在植物细胞自噬机制方面取得突破性进展,首次发现了植物自噬体膜的起源。有关研究可望为提高农业生产的质量提供新思路,研究成果已刊载于著名学术期刊《美国科学院院报》。
真核细胞具备自噬机制,会将自身的成分降解,回收作其他用途。自噬机制对很多细胞活动非常重要,特别是当细胞面对逆境或遭受病原体感染时,可发挥保护作用。2016年的诺贝尔奖得主大隅良典,就是凭解析细胞自噬作用机制而获奖。
在自噬过程中,一种名为自噬体(autophagosome)的细胞器,负责介导细胞内的物质运输到液泡或溶酶体作降解或重新利用。自噬体具有独特的双层膜结构,过去几十年来,研究细胞自噬机制的科学家们,一直致力于探寻自噬体膜的起源。负责调控自噬机制的蛋白称为核心自噬蛋白(ATG),植物的基因中包含了大部份的ATG,其中ATG9是唯一一个具备跨膜结构的核心自噬蛋白,因此长久以来被认为是自噬体膜的起源,惟一直未有确实的证据。
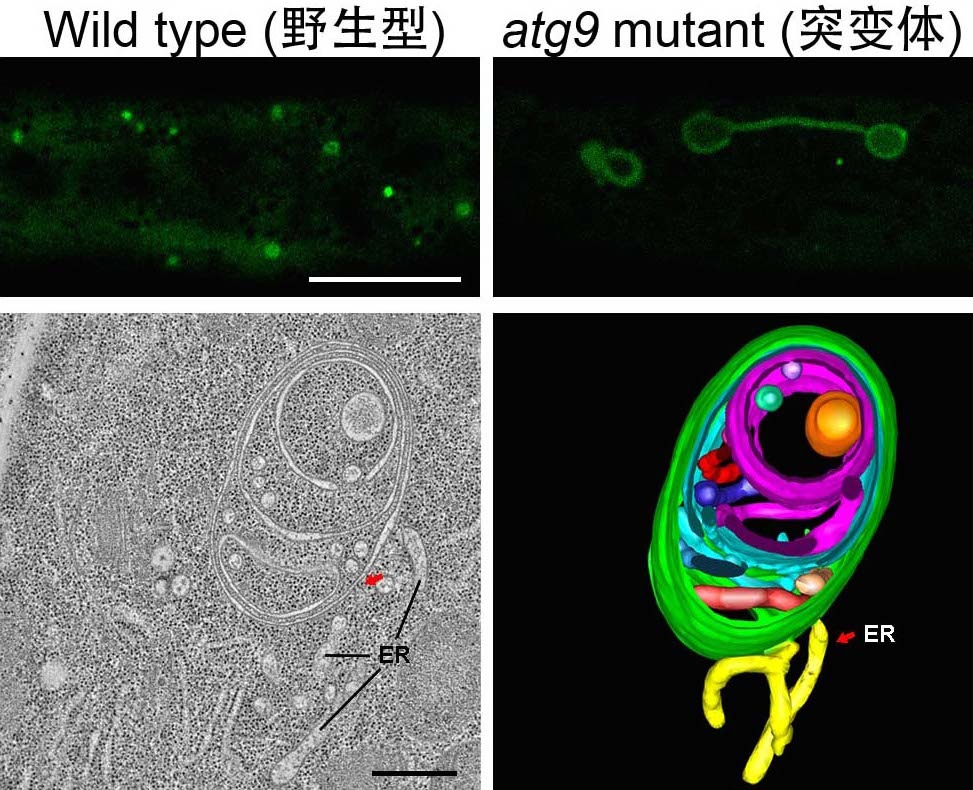
过去十六年来,中大姜里文教授的科研团队一直致力于研究蛋白质传输机理及细胞器的生物形成机制,在植物细胞生物学领域一直处于国际领先地位。内质网(endoplasmic reticulum, ER)是细胞内的一个精细的膜系统,是重要的细胞器。在是次发表于《美国科学院院报》的研究中,姜教授的科研团队发现了植物ATG9蛋白的独特功能──负责调控自噬体从内质网形成的过程,此发现直接证明了内质网是自噬体形成的起点。
研究自噬体起源的困难之处,在于需要仔细分析自噬体形成之初的结构及过程。姜教授的团队在研究中结合实时活体内成像、3D断层扫描电子重组技术和遗传学等方法,发现植物细胞中的ATG9基因缺失,会导致异常的自噬体小管形成,从而发现了植物ATG9蛋白,在自噬体从内质网形成的过程中所起的独特作用。
姜里文教授表示:「我们的研究对农业生产有潜在的应用价值。如何提升农作物的抗逆能力及抵抗病原体感染,是长久而艰巨的课题。ATG9蛋白在高等真核细胞中广泛存在,在水稻、玉米以及大豆等重要作物基因组都可以发现同源基因,因此植物自噬分子机理的相关研究,将可以为提高农作物质量等方面提供新思路。」
是次研究由姜里文教授团队中的两名博士后研究员庄小红博士和崔勇博士、博士研究生钟健奔,以及3D断层扫描电子显微镜专家姜秉昊教授合作完成。研究项目亦获得研究资助局卓越学科领域计划及协作研究金的拨款,以及中大细胞器生物合成和功能研究中心、细胞及发育生物学研究中心和农业生物技术国家重点实验室﹙香港中文大学伙伴实验室﹚的支持。
由姜教授指导的学生和博士后研究员多次荣获各项殊荣,包括两项中大青年学者论文奖、四项研究生最佳研究成绩奖、两项Keystone研讨会奖学金、两项国际人类前沿科学项目奖金和两次入选中国「青年千人计划」项目。